科研进展
《Nucleic Acids Research》发表谭俊杰教授团队“Engineering of high-precision C-to-G base editors with expanded site selectivity and target compatibility”
发布人: 发布日期: 2025-08-18 浏览次数:
碱基编辑器 (BE) 是无需 DNA 双链断裂或供体模板即可进行单核苷酸替换的强大工具。C 到 G 碱基编辑器 (CGBE) 的开发代表了一项重大进展,它能够实现碱基颠换,从而将遗传修饰的范围扩展到传统的转换之外,并促进更广泛的(治疗)应用。然而,目前的 CGBE 存在编辑范围受限的问题,主要修改相对于 PAM 远端的 6 位,并且其编辑效率取决于序列环境。
2025年8月11日,南京农业大学农学院谭俊杰唯一通讯在Nucleic Acids Research在线发表题为“Engineering of high-precision C-to-G base editors with expanded site selectivity and target compatibility”的研究论文。该研究通过系统地探索脱氨酶以构建 CGBE,我们鉴定出基于 PmCDA1 的 CGBE,它们优先编辑 3 位。此外,我们报告称,CDA1 C 端的截短显著提高了 C 到 G 的编辑效率。

CRISPR-Cas 系统作为细菌的适应性免疫系统,保护细菌免受病毒和质粒等侵入性核酸的侵害。它由一条向导 RNA (gRNA) 和一些 Cas 蛋白组成,gRNA 通过互补碱基配对识别靶位,而 Cas 蛋白通常包含两个核酸酶结构域,可以切割靶 DNA 的双链。来自化脓性链球菌的 Cas9 酶 (SpCas9) 因其成功的重新利用而被广泛用于基因组编辑。当 DNA 被切割时,会产生双链断裂 (DSB),随后通过细胞 DNA 修复机制进行修复,通常是非同源末端连接 (NHEJ)。NHEJ 是一种高效但易错的途径,存在于大多数细胞中,可导致靶位点的随机插入或缺失 (indel),因此常常通过产生功能丧失的等位基因导致基因敲除。
尽管基于 CRISPR-Cas 的工具能够有效地进行基因敲除,但它们在高效、精准地引入点突变的能力方面仍然有限,而点突变是基因治疗和精准育种所必需的(例如,50% 以上的人类遗传病是由于点突变引起的)。为了解决这个问题,研究人员一直致力于重新设计 CRISPR-Cas 系统,以引入序列特异性的 DNA 变化。其中一种方法是将 Cas 核酸酶与包含所需基因组改变且两侧是同源序列的外源 DNA 模板共同递送到目标位点,以激活细胞同源定向修复 (HDR) 途径,这是一种高保真度的修复机制。虽然 HDR 允许广泛的编辑,但在大多数细胞类型中,它的编辑效率通常较低。此外,HDR 需要提供供体 DNA 作为修复模板,而其他修复途径(如 NHEJ)也可能错误地利用该模板,从而产生意外突变。
自 2016 年以来,人们开发出了 CRISPR 碱基编辑器 (BE),它涉及催化受损的 Cas 核酸酶与核苷脱氨酶的融合。这使得引入点突变而无需供体 DNA 模板,也不会在目标 DNA 中造成 DSB。当前的 BE 主要实现同一组核苷酸内的碱基转换(即嘧啶到嘧啶或嘌呤到嘌呤的替换)。例如,可以使用胞嘧啶碱基编辑器 (CBE) 完成 C 到 T 的替换,而使用腺嘌呤碱基编辑器 (ABE) 完成 A 到 G 的转换。最近,建立了一种新型 BE,称为 C 到 G 碱基编辑器 (CGBE),它包含 Cas9 切口酶 (nCas9)、脱氨酶,有时还包括额外的尿嘧啶 DNA N-糖基化酶 (UNG)。特异性是通过将 gRNA 的 20 个核苷酸原型间隔序列与互补目标 DNA 精确配对来实现的,形成 R 环结构,然后脱氨酶将非目标链上的胞嘧啶转化为尿嘧啶,然后进行处理以生成所需的 C 到 G 碱基变化。尽管已经通过脱氨酶工程和/或与额外碱基切除修复 (BER) 蛋白融合做出了巨大努力来提高编辑效率和产品纯度(即所有编辑等位基因中仅包含所需编辑的比例),但目前可用的 CGBE 在其编辑范围方面受到严重限制,因为它们相对于原型间隔相邻基序 (PAM) 的远端选择性地编辑原型间隔内的位置 。此外,它们的有效性在很大程度上依赖于 DNA 底物的序列环境,表现出对富含 AT 的序列环境的强烈编辑偏好,这严重限制了 CGBE 的潜在应用范围。
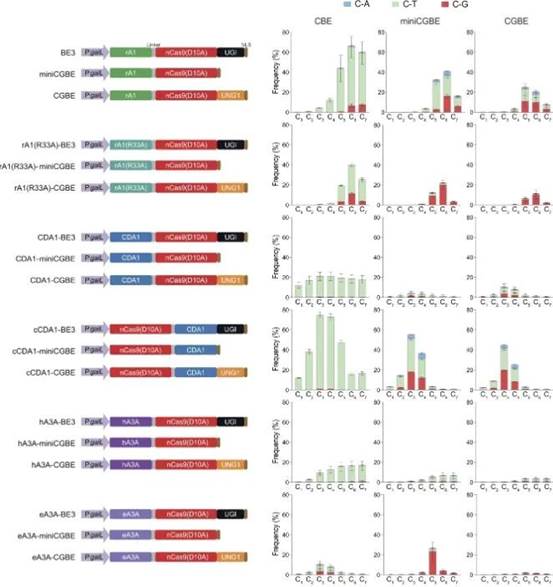
在本研究中,作者旨在通过构建一组功能更丰富、具有替代编辑窗口和更高靶点兼容性的 CGBE 来解决当前 CGBE 的主要局限性。为此,作者测试了几种脱氨酶(及其变体)与 nCas9 的融合,并确定了基于 PmCDA1(以下简称 CDA1)的 CGBE 具有替代编辑窗口。CDA1 CGBE 在 PAM 远端 3 号位置的编辑效率最高。此外,通过在 CGBE 中截短 CDA1 部分,作者能够进一步提高 C-to-G 编辑的效率和产物纯度。本研究还表明,新的 CDA1 CGBE 可以实现高精度的 C-to-G 编辑,同时与多种底物序列兼容。这些新型高精度 CGBE 显著扩展了 C-to-G 编辑的可能性,为基因治疗、精准育种和基础研究的应用提供了巨大的潜力。
- 上一篇: 《Cell Reports》发表许冬清教授团队“BBX10 interacts with PIF1 to prevent photo-oxidation and to promote the greening process”
- 下一篇: 《Computers and Electronics in Agriculture》发表姜东教授团队“High-throughput wheat seedling phenotyping via UAV-based semantic segmentation and ground sample distance driven pixel-to-area mapping”
